En resumen: Es falso que el Ministerio de Salud le haya solicitado a la empresa farmacéutica Pfizer la ampliación de la vida útil de las vacunas contra la COVID-19 que se aplican en el país. También es falso que la Caja Costarricense del Seguro Social (CCSS) haya distribuido vacunas caducadas. Ambas falsedades fueron propagadas por el Diario Extra desde el 31 de mayo pasado.
Diario Extra utilizó un comunicado del Ministerio de Salud de inicios de mayo que, en realidad, era un acuse de recibo a información enviada inicialmente por Pfizer. La casa farmacéutica informó a Salud de la autorización que dio la Administración de Alimentos y Medicamentos (FDA) de Estados Unidos para actualizar la vida útil de las vacunas anticovid de nueve a 12 meses en total, con base en estudios que respaldaron su estabilidad y eficacia.
Inicialmente, las vacunas de Pfizer/BioNTech recibieron la aprobación de uso de emergencia de la FDA con una vida útil de seis meses en congelamiento. La entidad reguladora aprobó extensiones de tres meses para las dos presentaciones de la vacuna de Pfizer (PBS y Tris/Sacarosa) en agosto y diciembre del 2021 respectivamente, que fueron reconocidas por el gobierno costarricense en septiembre del 2021 y enero pasado.
El medio de comunicación omitió ese hecho y publicó falsamente que las autoridades sanitarias “estaban recibiendo vacunas cuya fecha de vencimiento había caducado y posteriormente le fue ampliada”, refiriéndose a lotes almacenados por la CCSS en mayo, los cuales tenían impresa la fecha de vencimiento original (marzo de este año). Esas vacunas contaban con una ampliación de tres meses en su vida útil original.
El Ministerio de Salud confirmó a Doble Check que dicha institución “no solicita a los proveedores la ampliación en fechas de caducidad”. El ministerio aclaró que “son los proveedores los que, basados en los nuevos resultados de sus estudios y aprobaciones emitidas por la FDA, presentan la actualización ante el ente rector”.
Por su parte, la CCSS advirtió que las fechas de caducidad de las vacunas distribuidas en el país están definidas “a partir de la extensión dada por el fabricante a partir de los estudios de estabilidad” y que “las vacunas son utilizadas antes de que lleguen a su fecha de caducidad”.
¿Qué publicó Diario Extra?
Diario Extra publicó el 31 de mayo pasado que “Salud le pide a Pfizer ampliar vencimiento a vacunas Covid”. El periódico le atribuyó esa afirmación a Alexander Solís, quien fue presidente de la Comisión Nacional de Emergencias (CNE) durante la administración Alvarado Quesada. Diario Extra también dijo que, según Solís, las vacunas adquiridas por las autoridades sanitarias costarricenses “están vencidas”.
El medio de comunicación incluyó la transcripción de una entrevista a Solís. El texto carece de una cita textual que sostenga las atribuciones hechas por Diario Extra en la noticia sobre la supuesta petición de Salud a Pfizer.
La nota contiene un documento interno que el laboratorio de normas y calidad de la Caja Costarricense del Seguro Social (CCSS) envió a su área de almacenamiento y distribución el 13 de mayo del 2022. En la misiva, el laboratorio comunicó la actualización de las fechas de vencimiento en los informes de un conjunto de lotes de vacunas de Pfizer/BioNTech, con base en “documentos técnicos” presentados por Pfizer.
Algunos de los lotes detallados en este documento tenían a marzo del 2022 como “fecha de vencimiento consignada anteriormente”. El laboratorio de la Caja comunicó que la fecha actualizada para esas vacunas debía ser el 30 de septiembre de este año (seis meses más).
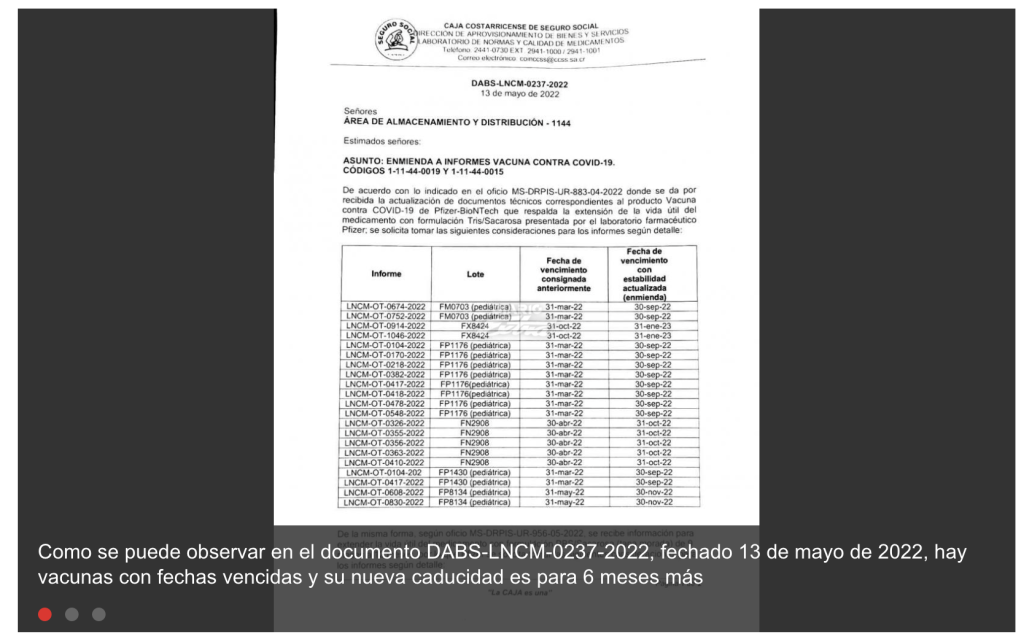
Al día siguiente, el periódico divulgó la primera página del oficio MS-DRPIS-UR883-04-2022 del Ministerio de Salud, en un artículo titulado como “CNE no advirtió a la población que recibía vacunas vencidas”. El medio afirmó que la población “estaba recibiendo vacunas cuya fecha de vencimiento había caducado y posteriormente le fue ampliada”.

Sin embargo, la nota incluyó la siguiente aclaración: “Alex Solís, expresidente de la Comisión Nacional de Emergencias (CNE), aclara que él nunca aseveró que se habían vencido las vacunas, únicamente confirmó que se había tramitado una ampliación a las fechas de vencimiento de los lotes para tener una nueva fecha de caducidad”.
Doble Check consultó a Diario Extra sobre el fundamento de la supuesta petición del Ministerio de Salud a Pfizer. La directora del medio de comunicación, Sandra Cordero, dijo únicamente que la noticia se basó en el oficio de Salud que fue publicado el 1 de junio.
Actualizaciones de vida útil de las vacunas
El ministerio de Salud no le pidió a Pfizer un cambio en las fechas de caducidad de las vacunas anticovid. En realidad, la empresa debe notificar este tipo de actualizaciones al gobierno, una vez que hayan sido aprobadas por la Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés) de Estados Unidos.
Inicialmente, las vacunas de Pfizer/BioNTech recibieron la aprobación de uso de emergencia de la FDA con una vida útil de seis meses en congelamiento. Pfizer aclaró a Doble Check que su laboratorio farmacéutico ha desarrollado dos presentaciones de la vacuna: PBS y Tris/Sacarosa.
La presentación PBS debe diluirse y se aplica a personas mayores de 12 años; su empaque tiene tapa morada y de cada vial se obtienen seis dosis. En cambio, la versión Tris/Sacarosa es distribuida en viales con tapa naranja que deben diluirse en diez dosis para su uso en niños de 5 a 11 años de edad; y en viales con tapa gris para mayores de 12 años (diluidos en seis dosis).
La FDA aprobó una extensión de tres meses adicionales en la vida útil de la presentación PBS de las inoculaciones el 24 de agosto del 2021 y para la versión Tris/Sacarosa en diciembre de ese mismo año, para un total de nueve meses. La entidad reguladora determinó que las dosis mantenían su integridad en ese plazo al mantenerse congeladas entre -90°C y -60°C.
Dichas ampliaciones fueron reconocidas por el gobierno de Costa Rica en septiembre del 2021 y en enero pasado (oficio MS-DRPIS-UR-102-01-2022), respectivamente. Así lo confirmaron Pfizer y la CCSS en respuestas oficiales a Doble Check.
La entidad reguladora de Estados Unidos permitió una extensión adicional en la vida útil de las vacunas el 13 y el 26 de abril de este año. De ese modo, las vacunas de Pfizer que cumplen los criterios establecidos tienen hasta 12 meses de vida útil actualmente. Pfizer le comunicó la nueva decisión y su fundamento técnico al Ministerio de Salud costarricense en mensajes enviados el 29 de abril y el 6 de mayo.
El documento utilizado por Diario Extra es un oficio donde el Ministerio de Salud confirmó la recepción de esa información técnica que envió Pfizer. El oficio MS-DRPIS-UR883-04-2022, del 3 de mayo, fue enviado por la evaluadora de medicamentos biológicos de Salud a la representante legal de Pfizer, Laura Rodríguez Arguedas, y se refiere a la presentación Tris/Sacarosa de la vacuna:
“Se recibe la notificación presentada a la FDA con la información que respalda la extensión de la vida útil del medicamento con formulación Tris/Sacarosa de 9 meses a 12 meses entre -90 a -60 °C, así como otras correcciones realizadas en las Hojas informativas para proveedores de la salud de la formulación Tris/Sacarosa para mayores de 12 años de la vacuna (vial con tapa gris) y para niños de 5 a 11 años (vial con tapa naranja) para alinearla a la versión aprobada por la FDA”, respondió la jerarca de Salud a Pfizer.
La ampliación de tres meses adicionales para la versión PBS de los viales de Pfizer fue reconocida por el gobierno costarricense el 9 de mayo en el oficio (MS-DRPIS-UR-956-05-2022).
El Ministerio de Salud confirmó a Doble Check que esa institución “no solicita a los proveedores la ampliación en fechas de caducidad”. Salud aclaró que “son los proveedores los que, basados en los nuevos resultados de sus estudios y aprobaciones emitidas por la FDA, presentan la actualización ante el ente rector”.
“Es el laboratorio quien notifica al Ministerio de Salud los cambios en los documentos técnicos del producto y hojas informativas autorizadas para la vacuna luego de que estos fueron notificados y aprobados por la FDA, como en este caso”, aseguró el Ministerio de Salud.
CCSS no aplicó vacunas vencidas
La actualización de la FDA de finales de abril determinó que los lotes de Pfizer que originalmente tenían impresa su expiración en marzo del 2022 debían ser actualizados para que el nuevo límite fuera el 30 de septiembre (seis meses más), considerando las dos ampliaciones en la vida útil de los medicamentos.
Esa es la misma indicación que el laboratorio de normas y calidad de la Caja le remitió a su área de almacenamiento y distribución el 13 de mayo, que Extra utilizó para decir falsamente que las vacunas ya habían caducado cuando se emitió el documento interno.
La CCSS aclaró a Doble Check que las vacunas contra la COVID-19 han sido distribuidas dentro de su vida útil. La institución detalló que la aplicación de las dosis está programada “a partir de las fechas de caducidad máximas, definidas a partir de la extensión dada por el fabricante a partir de los estudios de estabilidad”.
“Por consiguiente, las vacunas son utilizadas antes que lleguen a su fecha de caducidad. Como política institucional, ningún medicamento (incluidas las vacunas) es despachado y utilizado cuando ha superado su fecha de caducidad”, dijo la CCSS en una respuesta oficial.
¿Cómo se respalda la vida útil de las vacunas?
El Ministerio de Salud explicó que los laboratorios farmacéuticos deben hacer estudios de estabilidad, “en los cuales se evalúan las características físicas, químicas, biológicas o microbiológicas del medicamento durante el período de vencimiento, bajo condiciones controladas de almacenamiento”.
Esa institución destacó que la distribución de las vacunas de Pfizer/BioNTech inició respaldada por estudios de estabilidad a tiempo real a seis meses, “por lo cual esa fue la vida útil que se les aprobó inicialmente”.
“Pero estos estudios continuaban y conforme los laboratorios evidenciaban que el producto mantenía las características físicas, químicas, biológicas, y microbiológicas un par de meses, presentan esa actualización a las Agencias Reguladoras para su evaluación y aprobación”, agregó Salud.
La Caja recalcó que la aprobación de ampliaciones en la vida útil de las inoculaciones es una garantía de que “las vacunas y cualquier medicamento al que se le realicen estos estudios han demostrado que son estables y mantienen sus características de eficacia y seguridad durante el periodo estudiado”.
“Por consiguiente, son seguros de utilizar por el periodo de tiempo analizado”, añadió la CCSS en una respuesta a Doble Check.
Nota del editor: Esta verificación fue actualizada el 15 de junio del 2022 para incluir las declaraciones oficiales que Pfizer envió a Doble Check el 13 de junio. Esa respuesta detalló la diferencia entre las presentaciones PBS y Tris/Sacarosa de la vacuna y las fechas de actualización de la vida útil de ambas versiones.